Proteínas, aminoácidos e enzimas
INTRODUÇÃO
A respiração celular, o código genético e o processo metabólico são algumas dentre as funções vitais que ocorrem em nosso organismo. A respiração só é possível pela presença da Hemoglobina, que é responsável pelo transporte de oxigênio para as células do corpo humano. Adicionalmente, as enzimas controlam processos como a replicação do DNA e outras transformações do metabolismo.
As proteínas são moléculas constituídas por aminoácidos, de centenas a milhares destes, que se ligam um a um para formar a estrutura de macromolécula da proteína. Para entender melhor, imagine um certo número de indivíduos, que se ligam pelas mãos, para formar uma imensa cadeia de pessoas. Nesta analogia, cada pessoa seria um aminoácido (diferente um do outro), e a cadeia como um todo seria a molécula da proteína.
AMINOÁCIDOS E PROTEÍNAS
Aminoácidos podem ser entendidos separadamente, ou ligados a proteínas. Após ligação à proteína, ocorre uma pequena modificação em sua composição, a perda de dois átomos de hidrogênio e um de oxigênio (perda de água após realização da ligação peptídica), e a mudança de função química, que passa a ser amida. Entendamos a estrutura de um aminoácido fora do contexto de uma proteína.
Todo aminoácido pode contar com mais de dois grupos funcionais, porém dois sempre existirão em sua estrutura. O grupo amino (-NH2 ), e o grupo carboxila (-COOH), que caracterizam, respectivamente, as funções amina e ácido carboxílico. A presença dessas duas funções na mesma molécula esclarece a nomenclatura utilizada, “aminoácido”.
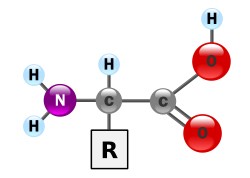 Molécula de aminoácido (Foto: Colégio Qi)
Molécula de aminoácido (Foto: Colégio Qi)
Observe na figura a presença de diversos grupos na composição dos aminoácidos. Cada molécula de aminoácido é composta de um átomo de C, que se ligará a um hidrogênio, a um grupo amino, a uma carboxila e a um grupo orgânico que chamaremos de resíduo. Este grupo residual difere de aminoácido para aminoácido e determina sua propriedade.
Existem 20 aminoácidos no total, sendo doze são naturais e oito, essenciais. Observe:
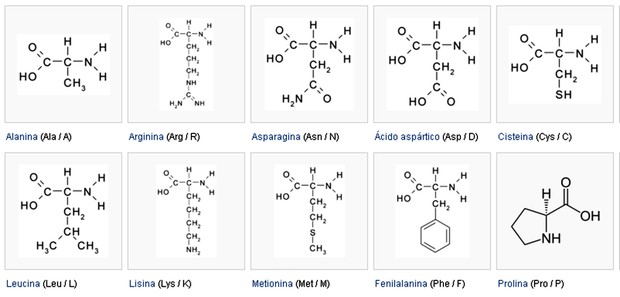 20 tipos de aminoácidos formadores de proteínas - parte I (Foto: Colégio Qi)
20 tipos de aminoácidos formadores de proteínas - parte I (Foto: Colégio Qi) 20 tipos de aminoácidos formadores de proteínas - parte II (Foto: Colégio Qi)
20 tipos de aminoácidos formadores de proteínas - parte II (Foto: Colégio Qi)
Aminoácidos naturais são aminoácidos já produzidos por nosso corpo, de forma natural. Aminoácidos essenciais são aminoácidos que não são produzidos por nosso corpo, e que devemos ingerir na alimentação para obtê-los.
Ligações peptídicas
Ligações peptídicas
A ligação peptídica ocorre com a liberação de um hidrogênio do grupo amino de um aminoácido, e da hidroxila do grupo carboxila do outro, liberando água (H2O ), e formando uma nova ligação, entre o N de um aminoácido e o carbono da carbonila do outro envolvido na reação. Note a figura abaixo, com o antes e o depois da formação da ligação. Esta ligação faz surgir um novo grupo funcional, que caracteriza a função amida na proteína.
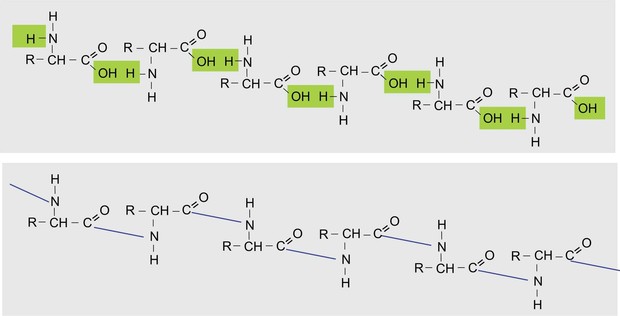 Processo de formação da ligação peptídica (Foto: Colégio Qi)
Processo de formação da ligação peptídica (Foto: Colégio Qi)
Estrutura
Quatro são os níveis para a estrutura de uma proteína. Estrutura primária, secundária, terciária e quaternária. A sequência linear de uma proteína caracteriza sua estrutura primária. Por exemplo, ...Val-Ser-Thr...
Obs.: Se a ordem dos aminoácidos mudar na ordem linear, a proteína será diferente. Uma proteína que contenha a sequência “Val-Hys-Val” no lugar de “Hys-Val-Val”, será diferente, com outras propriedades.
A forma como os aminoácidos interagem, com pontes de hidrogênio (interação física), ponte dissulfeto (ligação química) ou outros tipos, dependendo das propriedades dos resíduos de aminoácidos, irá determinar a forma segundo a qual cada “pedaço” da proteína irá se arranjar espacialmente (estrutura secundária). Duas são as formas possíveis, α-hélice ou β-pregueada.
O enrolamento destas formas irá determinar a estrutura terciária da proteína. Realizando-se uma analogia, este “enrolamento” é similar ao “emaranhado” dos fios antigos de telefone. A estrutura quaternária acontece quando duas ou mais proteínas se unem para desempenhar alguma função, como é o caso da hemoglobina. A figura formada pela interação das proteínas será a estrutura quaternária da proteína.
Obs.: Se a ordem dos aminoácidos mudar na ordem linear, a proteína será diferente. Uma proteína que contenha a sequência “Val-Hys-Val” no lugar de “Hys-Val-Val”, será diferente, com outras propriedades.
A forma como os aminoácidos interagem, com pontes de hidrogênio (interação física), ponte dissulfeto (ligação química) ou outros tipos, dependendo das propriedades dos resíduos de aminoácidos, irá determinar a forma segundo a qual cada “pedaço” da proteína irá se arranjar espacialmente (estrutura secundária). Duas são as formas possíveis, α-hélice ou β-pregueada.
O enrolamento destas formas irá determinar a estrutura terciária da proteína. Realizando-se uma analogia, este “enrolamento” é similar ao “emaranhado” dos fios antigos de telefone. A estrutura quaternária acontece quando duas ou mais proteínas se unem para desempenhar alguma função, como é o caso da hemoglobina. A figura formada pela interação das proteínas será a estrutura quaternária da proteína.
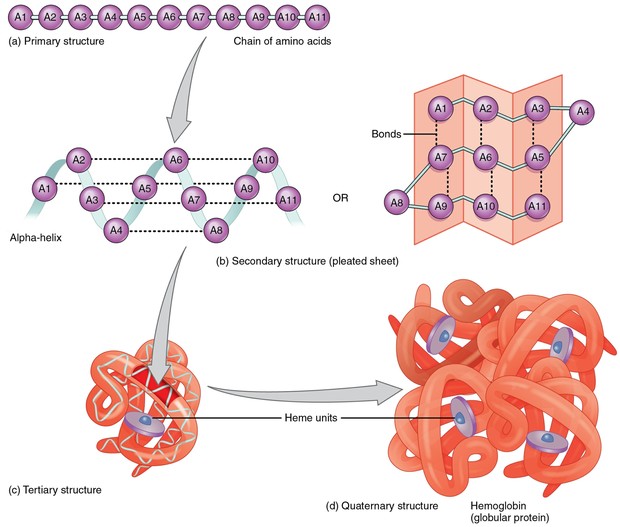 Níveis de estruturas proteicas (Foto: Wikipedia)
Níveis de estruturas proteicas (Foto: Wikipedia)
ENZIMAS
São proteínas que se ligam a substratos específicos e permitem a ocorrência de reações metabólicas por aceleração de suas velocidades. Essa especificidade entre substrato-enzima é usualmente associada ao modelo chave-fechadura, onde para cada “fechadura” (enzima), uma única “chave” (substrato) seria capaz de se ligar.
Fatores que afetam a atividade enzimática
Primeiro fator - temperatura: cada enzima tem uma temperatura ótima para sua atividade. Além disso, existem de temperatura, que, caso alcançado, provocam a desnaturação da proteína, uma alteração em sua forma que redunda em sua desativação. É válido lembrar que a forma da proteína é fundamental para o “encaixe” com o substrato.
Segundo fator - pH: cada enzima tem um pH ideal para atividade. Extremos de pH provocam a desnaturação da enzima, promovendo alterações em sua forma. O pH do estômago, por exemplo, apresenta o pH ideal para a atividade das enzimas digestivas ali presentes.
Terceiro fator - concentração de substratos: a atividade enzimática varia de acordo com a concentração de substrato disponível no meio. Considere duas situações: o substrato está em baixas concentrações. O substrato está em concentrações mais elevadas. O segundo caso será aquele que tenderá a apresentar a maior atividade enzimática, uma vez que é maior a concentração dos reagentes, com maior probabilidade de ocorrência para reação
Obs.: Existe uma concentração onde a atividade da enzima chega ao seu máximo. Isso significa que o aumento posterior da concentração de substrato não elevará a velocidade, uma vez que esta atingiu seu máximo.
EXERCÍCIOS
(Unifor-CE) Considere as afirmações abaixo relativas a enzimas:
I. São proteínas com função catalisadora;
II. Cada enzima pode atuar quimicamente em diferentes substratos;
III. Continuam quimicamente intactas após a reação;
IV. Não se alteram com as modificações da temperatura e do pH do meio.
I. São proteínas com função catalisadora;
II. Cada enzima pode atuar quimicamente em diferentes substratos;
III. Continuam quimicamente intactas após a reação;
IV. Não se alteram com as modificações da temperatura e do pH do meio.
São verdadeiras:
a) I e III apenas;
b) II e IV apenas;
c) I, III e IV apenas;
d) II, III e IV apenas;
e) I, II, III e IV.
a) I e III apenas;
b) II e IV apenas;
c) I, III e IV apenas;
d) II, III e IV apenas;
e) I, II, III e IV.
Gabarito
Letra A - Enzimas, que são proteínas com função catalisadora (aceleração de transformações bioquímicas), não modificam sua estrutura química após a ocorrência da reação.
Letra A - Enzimas, que são proteínas com função catalisadora (aceleração de transformações bioquímicas), não modificam sua estrutura química após a ocorrência da reação.
(UFMA) As enzimas, biocatalizadoras de indução de reações químicas, reconhecem seus substratos através da:
a) Temperatura do meio.
b) Forma tridimensional das moléculas.
c) Energia de ativação.
d) Concentração de minerais.
e) Reversibilidade da reação.
a) Temperatura do meio.
b) Forma tridimensional das moléculas.
c) Energia de ativação.
d) Concentração de minerais.
e) Reversibilidade da reação.
Gabarito
Letra B - A conformação da enzima é fundamental para um “encaixe” perfeito entre o substrato e a proteína (modelo chave-fechadura). Lembre-se que, ao desnaturar, as enzimas perdem sua forma e deixam de se ligar ao substrato, perdendo, assim, sua atividade.
Letra B - A conformação da enzima é fundamental para um “encaixe” perfeito entre o substrato e a proteína (modelo chave-fechadura). Lembre-se que, ao desnaturar, as enzimas perdem sua forma e deixam de se ligar ao substrato, perdendo, assim, sua atividade.
A ligação peptídica resulta da interação de dois grupos funcionais, originando um novo grupo funcional como produto de reação. Indique as funções envolvidas na reação, e a função originada.
Gabarito
O grupo amino de um aminoácido interage, reagindo, com o grupo carboxílico de outro aminoácido. A função originada na proteína é a função amida.
O grupo amino de um aminoácido interage, reagindo, com o grupo carboxílico de outro aminoácido. A função originada na proteína é a função amida.
Postado por Carlos PAIM
postado por Blog do Paim @ 10:16
0 Comentários
![]()


